摘要:水凝膠是細(xì)胞三維培養(yǎng)及組織體外構(gòu)建的最理想材料,顯然也是構(gòu)造器官芯片(微流控+微組織)的最理想平臺。然而目前的微加工工藝多用來加工硅、硅橡膠、聚合物等材料,迄今為止缺乏穩(wěn)定可靠的水凝膠微制造方法,這也嚴(yán)重制約了水凝膠在微流控芯片中的應(yīng)用。
有沒有可能發(fā)展出穩(wěn)定的水凝膠微流控芯片制造方法?這幾年課題組一直在探索有無可能基于全水凝膠構(gòu)造微流控芯片,并在這種高生物相容性的芯片上進(jìn)一步構(gòu)造出器官芯片,為器官芯片的制造提供全新的思路。
基于二次交聯(lián)的凝膠基微流控芯片制造工藝及原理
我們提出了一種制備水凝膠基微流控芯片的新方法:設(shè)計(jì)了芯片二次交聯(lián)策略,可實(shí)現(xiàn)具有任意復(fù)雜內(nèi)部流道的凝膠基三維微流控芯片的制造。該芯片的一個(gè)顯著特點(diǎn)是:不同層芯片間的鍵合強(qiáng)度和芯片本體一致。
我們采用常用的細(xì)胞三維培養(yǎng)用的水凝膠:海藻酸鹽、明膠、GelMA制造了水凝膠芯片,并對其機(jī)械性能及生物學(xué)性能進(jìn)行了系統(tǒng)的分析,研究發(fā)現(xiàn)采用課題組所產(chǎn)業(yè)化的GelMA生物水凝膠制造的芯片具有最佳的性能,可快速促進(jìn)芯片上細(xì)胞的功能化形成。
利用這種新型的水凝膠微流控芯片,我們建立了體外血管模型,CD31、Vinculin及Ve-Cadherin抗體染色表明,我們成功構(gòu)建出了接近體內(nèi)血管功能的血管芯片。隨后通過炎癥誘導(dǎo)因子的加載,模擬了動(dòng)脈粥樣硬化等病理?xiàng)l件下血管的炎癥反應(yīng)。本芯片可于組織血管化過程、心血管疾病、器官芯片、腫瘤藥物篩選等領(lǐng)域。
帶有復(fù)雜內(nèi)部流道的水凝膠芯片
浙江大學(xué)機(jī)械工程學(xué)院賀永教授課題組發(fā)明了一種基于二次交聯(lián)的凝膠基微流控芯片制造新方法,能夠構(gòu)造具有不同復(fù)雜內(nèi)部流道的凝膠芯片,進(jìn)而接種血管內(nèi)皮細(xì)胞,形成具有血管形態(tài)和功能的血管模型。通過凝膠基血管芯片的構(gòu)建不僅可以模擬血管的主要功能,還可以借助微流控手段施加各種流體剪切及生物因子的刺激。實(shí)現(xiàn)在時(shí)間和空間上重現(xiàn)體內(nèi)的血管環(huán)境,它可以應(yīng)用于血管化過程研究,心血管疾病研究,體外組織工程器官芯片的構(gòu)建,腫瘤藥物篩選等。本方法可實(shí)現(xiàn)微流道高強(qiáng)度封裝,便于物理剪切力、生物因子等施加刺激;同時(shí)水凝膠也為營養(yǎng)滲透以及分子擴(kuò)散提供了高效支撐。
相關(guān)論文Vessel-on-a-chip with Hydrogel-based Microfluidics近日刊登在WILLY旗下的Small雜志上。第一作者為聶晶博士生、高慶博士后、王怡棟生,通訊作者為賀永教授和轉(zhuǎn)化醫(yī)學(xué)院的陳偉教授。
一直以來,器官芯片的基底材質(zhì)通常是PDMS,塑料、硅等適合于微加工的材料,水凝膠可否作為微流控芯片的材料呢?我們設(shè)計(jì)了一種Bottom-Up的芯片制造策略,先加工出帶有微槽的水凝膠層(每層水凝膠含有兩種水凝膠材料,一種用于固化,一種用于后續(xù)的二次交聯(lián)),然后將水凝膠層堆疊拼裝,進(jìn)行二次交聯(lián),實(shí)現(xiàn)三維水凝膠微流控芯片制造。用這種方法,可制造帶有螺旋形流道、分叉流道、蛇形流道、多層互通流道等的水凝膠芯片。
基于二次交聯(lián)方法構(gòu)造的水凝膠基血管芯片
流道上的內(nèi)皮細(xì)胞逐漸貼壁,增殖,軸向及徑向布滿整個(gè)流道,自發(fā)對齊,形成網(wǎng)絡(luò)結(jié)構(gòu),流道開始實(shí)現(xiàn)血管化,Vinculin蛋白(一種細(xì)胞與細(xì)胞外基質(zhì)/細(xì)胞與支架之間相互作用的關(guān)鍵蛋白細(xì)胞)的表達(dá)驗(yàn)證了細(xì)胞與流道材料間聯(lián)系的產(chǎn)生,細(xì)胞間連接蛋白VE-Cadherin的表達(dá)表明了細(xì)胞之間形成緊密的相互連接,細(xì)胞之間實(shí)現(xiàn)明顯的交流,內(nèi)皮細(xì)胞功能蛋白CD31的表達(dá)進(jìn)一步驗(yàn)證了血管功能化的實(shí)現(xiàn)。此外,通過炎癥誘導(dǎo)因子的加載,模擬了動(dòng)脈粥樣硬化等病理?xiàng)l件下血管的炎癥反應(yīng)。
本方法的優(yōu)點(diǎn)有:
1.凝膠基微流控芯片的構(gòu)建得益于水凝膠材料的固有交聯(lián)性質(zhì),無需引入任何其他材料。
2.二次交聯(lián)原理可以應(yīng)用于任意具有不同交聯(lián)體系的水凝膠組合。
3.獲得的凝膠基微流控芯片沒有任何結(jié)合面分界線,完全結(jié)合為一個(gè)整體。4.方便構(gòu)建各種復(fù)雜形式的內(nèi)部流道。
5.具有良好的生物相容性,可以實(shí)現(xiàn)血管功能化。
-
芯片
+關(guān)注
關(guān)注
459文章
52158瀏覽量
436026 -
微流控
+關(guān)注
關(guān)注
16文章
576瀏覽量
19691
原文標(biāo)題:浙江大學(xué)賀永教授:水凝膠三維微流控芯片及在其上構(gòu)建的血管芯片
文章出處:【微信號:Microfluidics-Tech,微信公眾號:微流控科技】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
請問有沒有可能實(shí)現(xiàn)單電源供電的直流放大?
RT,這個(gè)圖標(biāo)有沒有可能不是函數(shù)里的,而是某個(gè)子VI?
有沒有可能是傳感器里面的MAX232芯片跟板子的232芯片不一...
有沒有可能在STM32MP1上實(shí)現(xiàn)網(wǎng)絡(luò)視頻流這個(gè)能力呢?
有沒有可能在IMX板上使用3個(gè)DSL 219攝像頭創(chuàng)建360度視圖?
基于微流控芯片的體外類生命系統(tǒng)
騰訊金融未來有沒有可能會(huì)獨(dú)立分拆,進(jìn)一步對接資本市場?
人到底有沒有可能戰(zhàn)勝人工智能
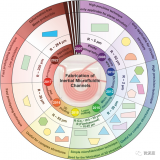
微流控技術(shù)中使用的不同類型的水凝膠
PDMS微流控芯片表面修飾的方法
基于顏色變化水凝膠的集成微流控壓力傳感






 有沒有可能發(fā)展出穩(wěn)定的水凝膠微流控芯片制造方法?
有沒有可能發(fā)展出穩(wěn)定的水凝膠微流控芯片制造方法?










評論