01
導(dǎo)讀
雖然鋰-空氣電池能夠提供高的能量密度,但在放電過程中形成的絕緣Li2O2阻礙了接下來的再充電過程。氧化還原介質(zhì)(RM)能夠促進(jìn)Li2O2氧化。低充電電壓下的快速動力學(xué)對于實際應(yīng)用是十分必要的,但尚未實現(xiàn)。
02
成果簡介
近日,Nature Chemistry上發(fā)表了一篇題為“Why charging Li–air batteries with current low-voltage mediators is slow and singlet oxygen does not explain degradation”的文章,該工作研究了RM氧化Li2O2的機(jī)理。結(jié)果表明限速步驟是Li2O2外層單電子氧化為LiO2,遵循Marcus理論。第二步以LiO2歧化為主,主要形成三線態(tài)O2。單線態(tài)O2的產(chǎn)率取決于RM的氧化還原電位,而與電解質(zhì)降解無關(guān)。該機(jī)制解釋了為什么目前的低壓介質(zhì)(<+3.3 V)不能提供高的充電速率(最大速率在+3.74 V),并提出了重要的介質(zhì)設(shè)計策略,以在更接近Li2O2氧化熱力學(xué)電勢(+2.96 V)下提供足夠高的速率進(jìn)行快速充電。
03
關(guān)鍵創(chuàng)新
該文章研究了氧化還原介質(zhì)氧化Li2O2的機(jī)理。
04
核心內(nèi)容解讀
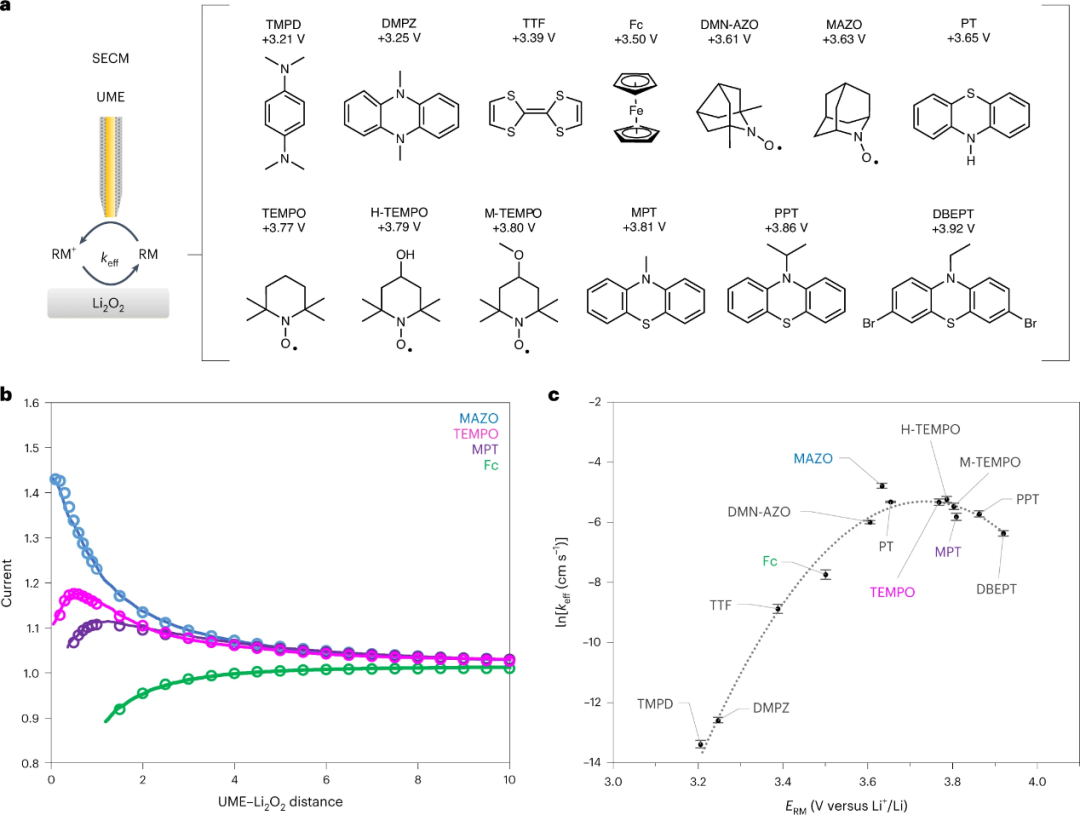
圖1、a,在SECM設(shè)備中使用的UME示意圖(左),以及所用RM的分子結(jié)構(gòu)和ERM值(右)。b,繪制的RM的Li2O2的SECM逼近曲線。c, 在0.1 M LiTFSIin四乙二醇二甲醚中,lnkeff隨ERM變化的Marcus曲線。@Nature
Marcus理論解釋RM動力學(xué)
為了研究Li-O2電池在充電過程中通過RM(式(1))氧化Li2O2的機(jī)理,使用具有不同氧化還原電位(ERM)的RM(從+3.2 V到+3.9 V)對該反應(yīng)的速率常數(shù)進(jìn)行了測量(圖1a)。
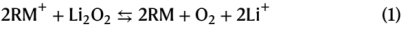
因此,得到了整個反應(yīng)的有效速率常數(shù)(keff),該反應(yīng)將由速率決定步驟主導(dǎo)。掃描電化學(xué)顯微鏡(SECM)廣泛用于定量測量非均相電子轉(zhuǎn)移速率常數(shù)。在本工作中,SECM采用圖1a所示的裝置來測量氧化的氧化還原介質(zhì)RM+與Li2O2反應(yīng)的keff。這可以通過繪制逼近曲線來實現(xiàn),其中超微電極(UME)逐漸逼近Li2O2基底。RM在UME被氧化成RM+,然后與Li2O2基底反應(yīng),產(chǎn)生一個反饋回路,電流隨距離而變化。圖1b為所選RMs的反饋逼近曲線,其中在較低的UME-Li2O2距離下,較高的電流代表較高的keff。在Li2O2氧化的一系列步驟中(式(2)-(6)),keff與決速步驟的速率常數(shù)成正比。TMPD和DMPZ的keff值太低,無法通過SECM測量,因此使用壓力傳感的方法測量,其中Li2O2和RM+混合在氣密室中,測量O2演變導(dǎo)致的壓力變化。
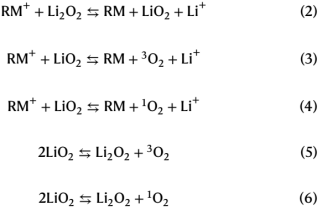
對于RM,將lnkeff數(shù)據(jù)繪制為ERM的函數(shù),得到如圖1c所示的火山狀圖。圖1c中的曲線形狀表明Marcus理論中電子轉(zhuǎn)移速率常數(shù)(ket)的表達(dá)式如式(7)所示。
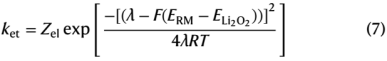
式中keff與ket成正比,ELi2O2為Li2O2的氧化還原電位,Zel為指前常數(shù),λ為重組能,F(xiàn)為法拉第常數(shù),R為氣體常數(shù),T為溫度。λ在不同RM上的變化很小,因為它們的分子體積相似。將方程(7)擬合到圖1c的數(shù)據(jù)中,可以看出keff隨ERM的變化與Marcus理論預(yù)測的趨勢一致。這意味著速率決定步驟是一個單一的外電子轉(zhuǎn)移過程。
擬合值為:ELi2O2=+3.41 V,λ=0.322 eV, Zel=0.00495。Li2O2是由Li+配位的離散O22?分子組成的寬帶隙固體。可以通過改變電解質(zhì)環(huán)境來改變重組能(λ),其中含有四丁基銨(TBA+)鹽的乙二醇二甲醚溶劑比堿金屬鹽的λ更大,這是由于它們的介電常數(shù)差異導(dǎo)致。
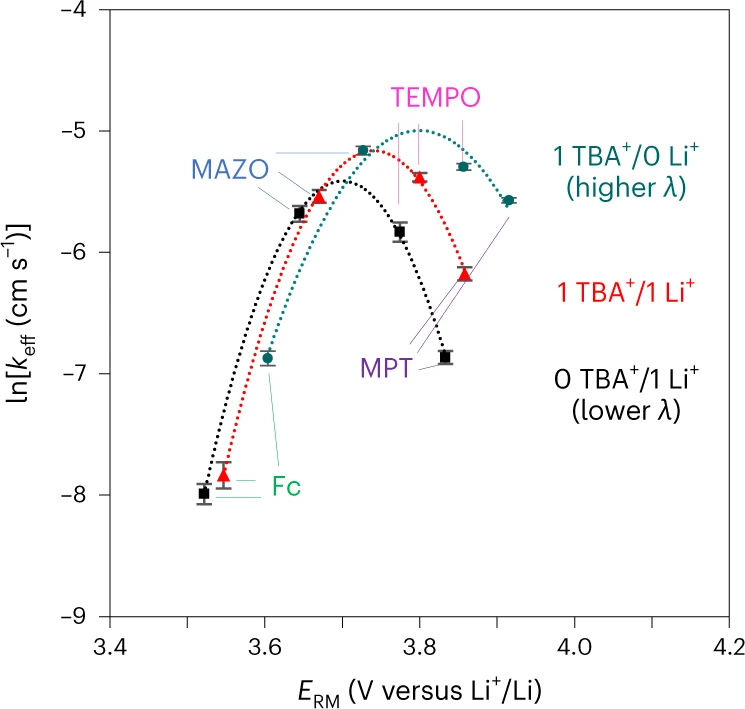
圖2、當(dāng)TBA+/Li+的總濃度保持不變時,lnkeff(RM+與Li2O2的反應(yīng))隨ERM的變化曲線。@Nature
圖2顯示了lnkeff隨各種電解質(zhì)成分ERM的變化,其中Li+越來越多地被TBA+取代,導(dǎo)致Marcus火山圖隨著TBA+濃度的增加而向右移動。根據(jù)Marcus理論(方程(7)),火山的頂點(即最高氧化速率)發(fā)生在FΔE=λ處。因此,隨著λ的增加,火山向更正的ERM移動。火山區(qū)域的擴(kuò)大也與λ的增加相一致。這些結(jié)果進(jìn)一步表明,RMs氧化Li2O2的動力學(xué)可以用Li2O2向RM+的外層單電子轉(zhuǎn)移來解釋。
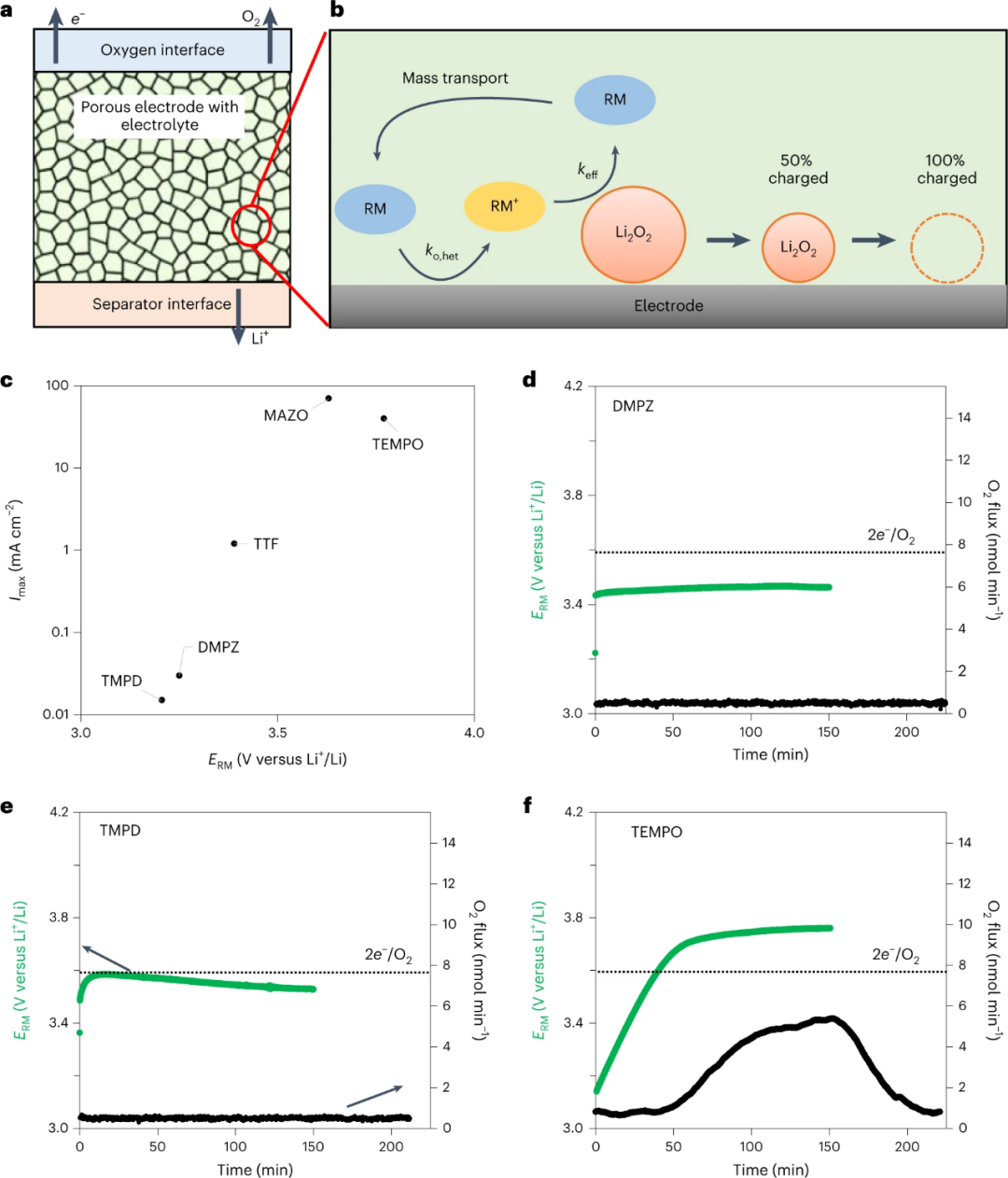
圖3.a,用于計算具有RM的鋰-空氣電池恒流充電的多孔正極模型示意圖。b、隨著氧化的進(jìn)行,顆粒尺寸減小。c,根據(jù)a中的正極模型,達(dá)到99.75%荷電狀態(tài)的Imax隨ERM的變化。d-f,預(yù)載Li2O2的Li-O2正極恒流充電曲線,使用1 M LiTFSI in 四乙二醇二甲醚電解質(zhì),添加10 mM DMPZ(d),10 mM TMPD(e)和10 mM TEMPO(f),并與在線質(zhì)譜儀相結(jié)合,用于檢測逸出的氧。@Nature
熱力學(xué)上,對于電勢>+2.96的任何介質(zhì),Li2O2都可能被氧化。然而,這并沒有回答實際充電速率需要多少過電位的問題。接下來,使用如圖3a、b所示的鋰離子電池多孔正極模型,以及為每種介質(zhì)確定的keff和ERM,模擬恒流充電曲線,以確定電池的充電速率極限。圖3c顯示了不同RM實現(xiàn)99.75%充電狀態(tài)的最大充電速率(Imax)。RM在電極表面的氧化速率(ko,het)和RM在表面與Li2O2顆粒之間的傳質(zhì)速率很快,因此限制速率的步驟是Li2O2被RM+氧化的過程。圖3c的結(jié)果表明,在極化到+4 V之前,較低電壓的RM只能以較低的速率維持充電。例如,DMPZ和TMPD實現(xiàn)>99%充電容量的最大充電速率≤0.1?mA?cm?2。相比之下,對于MAZO或TEMPO等高電壓介質(zhì),可以在≥40 mA cm-2充電。
接下來,通過對連接到在線質(zhì)譜儀的Li-O2電池充電,定性驗證了該模型的結(jié)果。圖3f顯示,含有TEMPO的電池可以充電并產(chǎn)生大量氧氣。相比之下,圖3d,e顯示,含有DMPZ或TMPD的電池只氧化RM,沒有檢測到任何氧氣釋放。對于后一種電池,雖然可以在電極表面直接氧化Li2O2,但電極是通過滴涂制備的,接觸不良,加上介質(zhì)動力學(xué)緩慢,電極中Li2O2含量相對較少,O2的析出被抑制在+4 V以下。
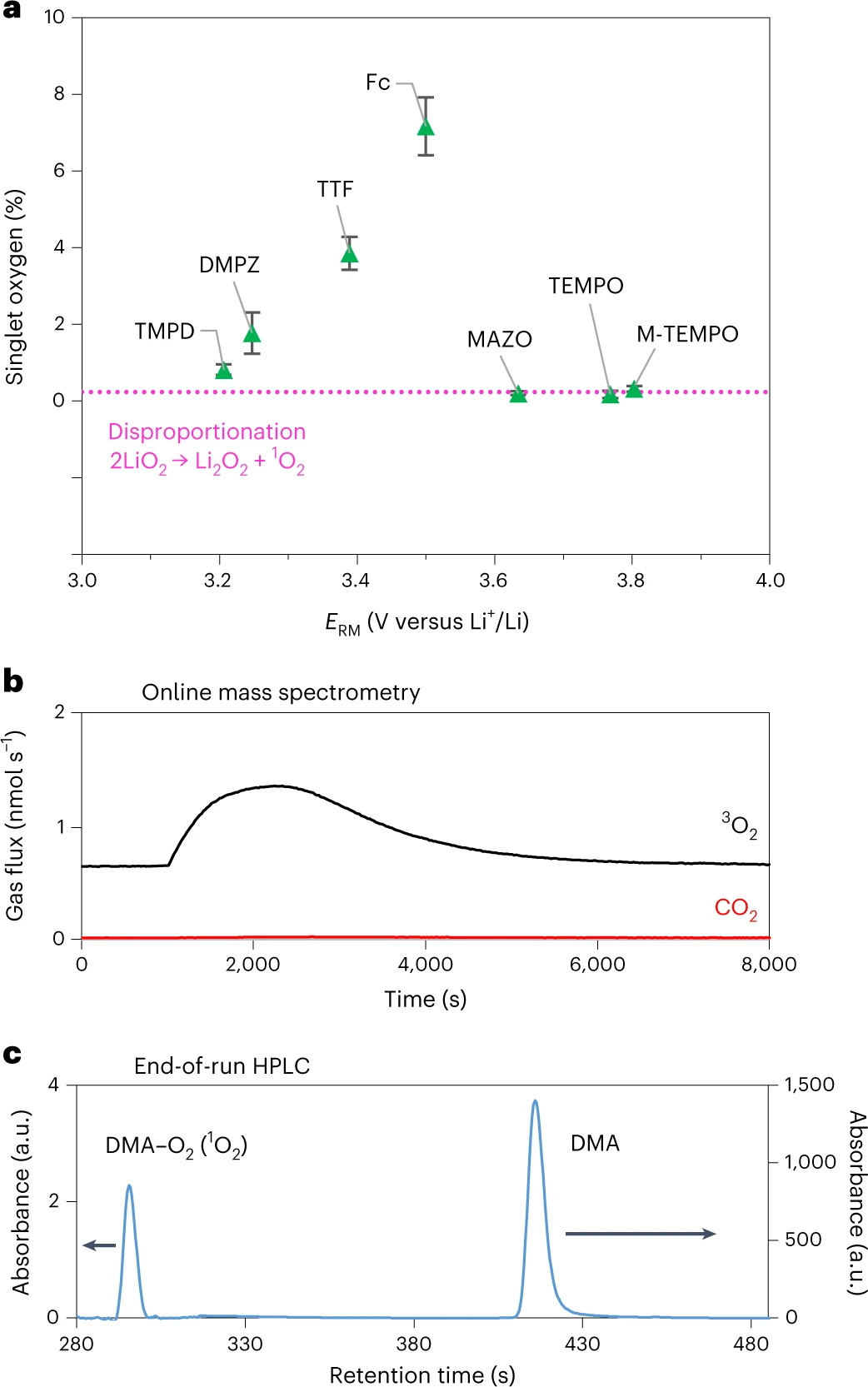
圖4.a,單線態(tài)氧的產(chǎn)率(1O2/(1O2+3O2)百分比)隨氧化還原電位(ERM)的變化,以及與LiO2歧化產(chǎn)率的比較(虛線)。b,從TEMPO+與Li2O2反應(yīng)容器頂部空間取樣的氣體產(chǎn)物(黑色的3O2和紅色的CO2)的在線質(zhì)譜檢測。c、通過對TEMPO+與Li2O2完全反應(yīng)的液體溶液取樣進(jìn)行HPLC分析。@Nature
單線態(tài)氧的演化及反應(yīng)機(jī)理
Li2O2首先氧化生成LiO2(式(2))。然后,LiO2通過兩種途徑,即LiO2氧化(式(3)和(4)或LiO2歧化(式(5)和(6)),以三線態(tài)(3O2)或單線態(tài)(1O2)的形式變成O2。總的Li2O2氧化反應(yīng)應(yīng)導(dǎo)致電荷/氧比例為e?/O2=2。然而,該值通常>2,這表明存在副反應(yīng)。這種副反應(yīng)歸因于電解質(zhì)溶液或碳正極受到反應(yīng)性O(shè)2的攻擊。之前的研究已經(jīng)證明充電電壓會影響1O2產(chǎn)率(即1O2/(1O2+3O2))。在這項研究之前,研究人員已經(jīng)探索了用RMs給鋰氧電池充電的O2產(chǎn)量。本工作通過將Li2O2與四烯胺中化學(xué)氧化的RM(RM+)混合來量化1O2產(chǎn)率,以了解RM+氧化在1O2產(chǎn)率中的作用。這個分析也使得能夠確定式(2)-(6)中哪一個步驟限制了Li2O2的整體氧化速率。結(jié)果如圖4所示。使用在線質(zhì)譜法測量3O2的量,而1O2的量通過將其捕獲在9,10-二甲基蒽(DMA)溶液中來測量,DMA是一種選擇性化學(xué)陷阱,可與1O2快速反應(yīng)形成DMA內(nèi)過氧化物(DMA-O2),然后使用高效液相色譜法(HPLC)定量(圖4c)。圖4a顯示了每種介質(zhì)的1O2產(chǎn)率隨ERM的變化。為了確定LiO2化學(xué)歧化直接產(chǎn)生1O2的產(chǎn)率,將超氧化鉀(KO2)與含有Li+和18-冠-6-醚的四乙二醇二甲醚溶液混合,通過式(5)和式(6)誘導(dǎo)LiO2自發(fā)歧化。1O2產(chǎn)率為0.23%,如圖4a中粉色虛線所示。圖4a顯示,對于ERM在3.2~3.5 V之間的RMs,1O2產(chǎn)率高于LiO2歧化產(chǎn)生的1O2產(chǎn)率,而對于ERM≥3.6 V的RMs,1O2產(chǎn)率是恒定的(與LiO2歧化的1O2產(chǎn)率一致),與電位無關(guān)。
由圖1可知,Li2O2氧化的決速步驟是第一或第二單電子氧化,即Li2O2→LiO2或LiO2→1O2或3O2。在圖4a中,LiO2歧化產(chǎn)生的多余1O2一定來源于第二電子轉(zhuǎn)移,即LiO2氧化生成1O2(式(4))。對比圖1中keff的變化趨勢(即Li2O2氧化過程中限速步驟的有效速率常數(shù))與圖4a中形成的1O2比例變化趨勢,可以明顯看出,限速步驟不是RM++LiO2→RM+1O2+Li+,因為Li2O2氧化最大速率(圖1)對應(yīng)的電位與圖4a中最高的1O2比例并不一致。事實上,在最大的keff下,僅通過歧化就可以形成1O2。根據(jù)類似的論點,可以排除RM++LiO2→RM+3O2+Li+是決速步驟。因此,限速步驟是Li2O2的第一電子氧化:RM++Li2O2-RM+LiO2+Li+(式(2))。圖4a中O2的產(chǎn)率表明O2的主要產(chǎn)物是3O2,因此LiO2氧化或歧化的主要產(chǎn)物是3O2而不是1O2。圖4a還顯示,RM++LiO2→RM+1O2+Li+發(fā)生在3.2-3.5 V的ERM下,曲線的形狀表明,RM介導(dǎo)的LiO2氧化也可能遵循Marcus關(guān)系。基于這一假設(shè),可以預(yù)測3O2的能量比1O2低0.97 eV,即RM++LiO2→RM+3O2+Li+發(fā)生在<+2.96 V。這意味著在Li2O2被氧化的所有電位下,RM++LiO2→RM+3O2+Li+已經(jīng)反應(yīng)完畢。RM++LiO2→RM+1O2+Li+通過歧化途徑爭奪LiO2。隨著RM電位的增大,Li2O2氧化生成LiO2的速率加快,LiO2濃度升高,RM+濃度降低,有利于LiO2歧化。簡而言之,參與RM++LiO2→RM+1O2+Li+反應(yīng)的LiO2和RM+的量不是一個常數(shù)。
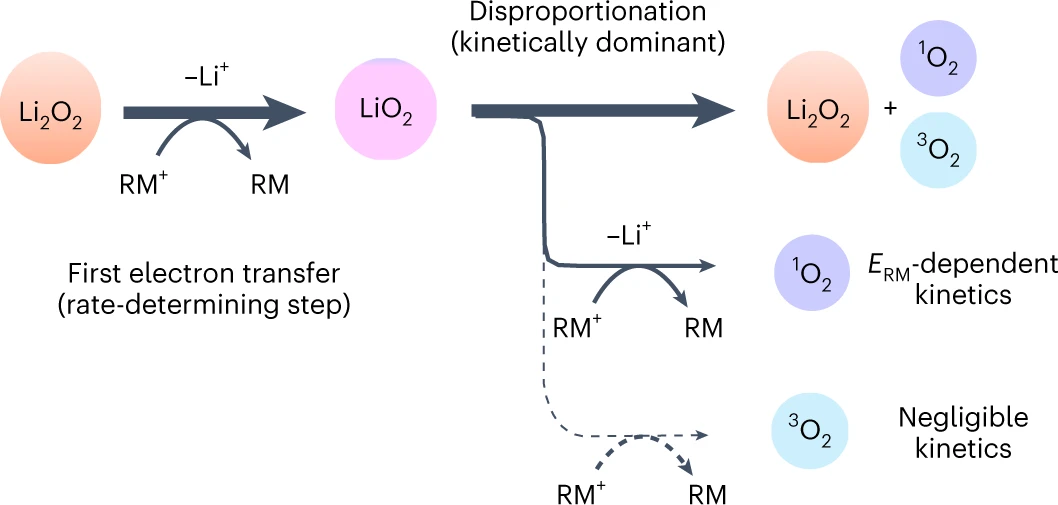
圖5.RM促進(jìn)Li2O2氧化反應(yīng)機(jī)理示意圖。@Nature
總之,Li2O2氧化的限速步驟是Li2O2的外層單電子氧化生成LiO2(式(2)),第二步是LiO2歧化生成3O2(式(5))。總體機(jī)理如圖5所示。
05
成果啟示
本文對Li2O2氧化機(jī)制的理解解釋了為什么在低電勢(<+3.3 V)下工作的介質(zhì),具有的良好往返能量效率,卻不能提供足夠高的充電速率。最優(yōu)的RM是在低電勢下充電的RM(也就是說,剛好足以在+3 V左右的熱力學(xué)條件下驅(qū)動反應(yīng)),并且具有快速的動力學(xué)和最少的反應(yīng)性1O2形成。然而,在+3.7 V左右的ERM下才能獲得最高的速率。考慮到限速步驟遵循Marcus動力學(xué),對于接近ELi2O2的低電壓RM,通過最小化重組能λ來降低活化能,有望實現(xiàn)快速的Li2O2氧化動力學(xué)(keff)。計算模型表明,氧化還原電位為+3.4 V的RM可以實現(xiàn)1 mA?cm?2的充電速率。本文的分析表明,當(dāng)ERM約為+3.45 V時,RMs的反應(yīng)性1O2生成量達(dá)到最大值,但當(dāng)ERM低于+3.2 V時,1O2的生成量接近基線值(即通過歧化生成的量)。因此,低電壓RM也將使1O2生成量最小化。對于在產(chǎn)生1O2量最多的電位(約為+3.45 V)下工作的RMs,e-/O2比例接近2,這與在產(chǎn)生1O2量較少的電位下工作的RMs的e-/O2比例非常相似。此外,Li-O2電池充電過程中的降解和副反應(yīng)在3.6 V以上最為顯著,此時1O2釋放最低。這些結(jié)果表明,在充電過程中,1O2可能不是副反應(yīng)的主要來源。
審核編輯:劉清
-
鋰電池
+關(guān)注
關(guān)注
260文章
8362瀏覽量
174901 -
電池充電
+關(guān)注
關(guān)注
9文章
466瀏覽量
74806 -
電解質(zhì)
+關(guān)注
關(guān)注
6文章
821瀏覽量
20587
原文標(biāo)題:牛津大學(xué)Nat. Chem.:揭秘鋰氧電池充電慢的根本原因
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
國產(chǎn)SiC碳化硅MOSFET廠商絕口不提柵氧可靠性的根本原因是什么
當(dāng)S32K312進(jìn)入睡眠狀態(tài)時,它會重置是什么原因導(dǎo)致的?
IGBT高溫漏電流和電壓阻斷能力固有缺陷是其被淘汰的根本原因
鋰電池充電器和鉛酸電池充電器怎么區(qū)分?有和不同?
主動靜電與漏電防御策略是全面消除整個電子制造過程中的工藝及品質(zhì)盲點的最佳策略

探究全電池容量衰減的根本原因
全固態(tài)鋰金屬電池的鋰陽極夾層設(shè)計





 揭秘鋰氧電池充電慢的根本原因
揭秘鋰氧電池充電慢的根本原因










評論